研究
婦人科腫瘍研究室
臨床腫瘍・臨床遺伝部門
婦人科がんに対する個別化医療および新規治療開発、遺伝性腫瘍に対するがん予防を主なテーマにしています。
Translational researchでは、臨床現場での実用化を目指します。Clinical researchでは、治療ガイドラインに貢献できる質の高いエビデンス作りを目指します。
当研究室では婦人科腫瘍専門医、細胞診専門医、内視鏡技術認定医、臨床遺伝専門医、遺伝性腫瘍専門医などの育成や、女性健康維持研究室とも連携して、女性ヘルスケア専門医の育成にも力を入れています。

基礎研究/Translational research
1.婦人科がんprecision medicineの推進
当研究室ではバイオバンク部門(Keio Women’s Health Biobank:KWB)のヒト試料のオミクス解析データを臨床情報とともに読み解くことで、がんの診断、治療および予防に直結する研究を行っています。ゲノム解析・リキッドバイオプシー・オルガノイドを用いた薬剤感受性試験など、複数の国内外の研究グループとの共同研究を推進しています。
2.新規バイオマーカー検索およびオルガノイド培養
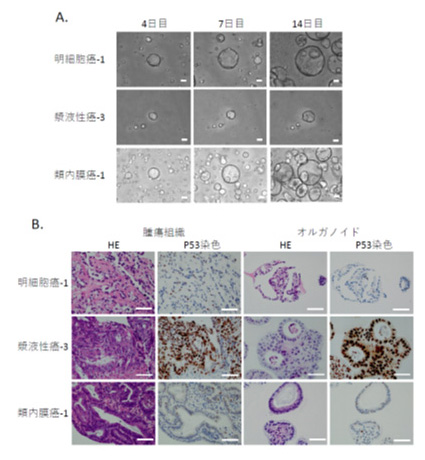
オルガノイドとは生体内の組織や臓器を解剖学的かつ機能的に高度に再現した3次元構造の”ミニ臓器”です。本研究室では、患者由来の卵巣癌組織検体から卵巣癌オルガノイドを樹立および株化に成功しました。オルガノイドと元腫瘍検体は組織学的にもゲノム解析でも類似しており、また腫瘍不均一性を保持しています。今後、最適な薬剤選択などの観点から個別化医療への展開が期待され、研究を進めています。
3.婦人科がん化学療法の効果および毒性の早期予測システムの開発
がん個別化医療への応用をめざし、婦人科がんに対し標準的に用いられるタキサン+プラチナ療法を中心に、抗がん剤の効果および毒性を早期に予測する手法の開発に取り組んでいます。遺伝子発現のみでなく細胞機能の変化を網羅的に解析可能な技術である“細胞アレイ”を利用し、抗がん剤の効果を予測できる標的遺伝子の探索を試みています。さらにゲノム薬理学の手法を用いて、抗がん剤の反応に関与する一塩基多型(SNP)の抽出も進めています。
4.若年性子宮体癌の予後予測因子の解明
がんの発生機序としてDNAメチル化が寄与することが知られています。当研究室では、病理学教室と協力して、子宮体癌のゲノム網羅的DNAメチル化解析を行い若年性子宮体癌におけるDNAメチル化プロファイルの研究をしております。プロファイルによる層別化を用いた治療計画も検討しております。また、若年性子宮体癌の子宮温存療法において予後予測因子を探索しています。免疫組織化学染色や、子宮体癌に特徴的な遺伝子変異に着目し、新たな予後予測因子の解明を目指しています。
5.婦人科バイオバンク (Keio Women’s Health Biobank)

慶應義塾大学医学部産婦人科はバイオバンク(Keio Women’s Health Biobank:KWB)を有しています。患者さんのご同意をいただいた後に組織検体、組織検体から作成したオルガノイド、血液由来試料とそれにともなう臨床情報や家族歴などを採取・保管しています。これらの生体試料・臨床情報は病気の原因解明、新たな診断・予防のためのバイオマーカー開発、婦人科疾患の新たな治療法の開発、などの研究に活用されます。現在、これらの試料をもとに国内外の複数の研究室と共同研究を実施しています。
http://www.obgy.med.keio.ac.jp/clinical/clinicalstudy.php#KWB
6.上皮-間葉転換 (Epithelial-Mesenchymal Transition (EMT))を標的とした新規がん治療の開発
子宮体部癌肉腫の肉腫成分はEMTとされ、癌肉腫はEMTを可視化できる貴重な腫瘍で、転移浸潤のモデルとなる。我々は癌肉腫のオミックス情報より、癌肉腫は癌より肉腫に類似していることを見出し、新規EMT関連遺伝子候補を抽出している。当該遺伝子の機能を解析し、新規EMT関連遺伝子を同定する。
7.腫瘍-間質作用の相互理解
腫瘍特性を規定する因子として、腫瘍細胞だけでなく間質細胞も重要である。我々はこれまで、卵巣がんおよび子宮体がんの腫瘍実質と間質をmicrodissectionで分離後、それぞれで発現解析を施行し、腫瘍-間質相互作用の側面から薬剤感受性および再発と関与する遺伝子を選別し、その一部は特許申請した。現在、当該遺伝子の機能を解析するとともに、体癌の再発を予測できる診断システムを開発している。
臨床研究/Clinical research
1. 若年性子宮体癌の子宮温存療法(黄体ホルモン療法)
我々は、若年子宮体癌患者に対し、高用量黄体ホルモン(酢酸メドロキシプロゲステロン、MPA)療法により女性の生殖機能を温存する治療を行っています。現時点で370症例以上に実施し多数例で妊娠に至っており、本邦でトップクラスの臨床経験を有しています。豊富な臨床経験を元に、本治療に関する臨床病理学的因子との関連を後方視的に解析するとともに、分子生物学的手法による治療効果判定や再発の早期発見を志向した研究を行っています。
2. 早期子宮体癌に対するセンチネルリンパ節ナビゲーションシステムの確立
原発巣の癌組織からのリンパが最初に流入するリンパ節をセンチネルリンパ節(SN)といいます。SNは種々の癌種でその同定に、術式や術後療法の選択に臨床的有用性があると言われています。我々は、主に子宮体癌において最適なSNの同定法(ラジオアイソトープ法、色素法、蛍光法)および診断法(免疫組織化学染色、捺印細胞診など)を研究しております。 また、SNに転移がない場合、リンパ節郭清を省略することが可能か検証する臨床試験も計画しています。
3. 遺伝性腫瘍に関する研究
婦人科腫瘍の一部は遺伝性腫瘍としての性格を有しています。我々は臨床遺伝学センター等と共同で遺伝性婦人科癌に関する研究と臨床を行っています。遺伝カウンセリングの後に、希望例に対しては遺伝学的検査や、リスク低減手術を行っています。また国内外のデータベースに対するデータシェアリングにも積極的に寄与することも目指しています。さらに女性健康維持研究室と共同してリスク低減手術後の女性QOLの課題についても取り組んでいます。
4.腹腔鏡下手術と低侵襲治療の確立
本学の医学教育統括センターに設置されている 臨床医の解剖学教育および研究施設であるClinical Anatomy Laboratory (CAL)において、未固定献体を用いた腹腔鏡下手術シミュレーションを重ね、高難易度の腹腔鏡下手術の安全な導入を推進しています。子宮体癌に対する腹腔鏡下手術においては、センチネルリンパ節ナビゲーション手術を応用したさらなる低侵襲手術に向けた研究を進めています。さらに若手医師を対象とした動物実習を毎年行っており、当教室全体の腹腔鏡下手術の手技向上に努めております。
5. 癌登録データなどを用いた疫学研究
日本産科婦人科学会のデータベース事業として、毎年全国の日本産科婦人科学会腫瘍登録参加施設から子宮頸癌、子宮体癌、卵巣癌の患者さんの臨床情報が匿名化され集積されています。数万におよぶ多数の患者さんのデータを扱い、進行期分類や組織分類、治療成績などについて統計解析を行い、日本国内の婦人科腫瘍の診断や治療に関して、海外の報告との比較検討を行います。
6. がん薬物療法と臨床試験
臨床の現場から出たクリニカルクエスチョンに答える臨床研究や、分子標的治療薬などを用いた新規治療の開発を目的とした前向き臨床試験に積極的に取り組んでいます。がん薬物療法では科内のリーダー的役割を担うとともに、企業治験の受託、他診療科との連携も進めています。JGOG(婦人科悪性腫瘍研究機構)、JCOG(日本臨床腫瘍研究グループ)、NRG Oncology (Gynecologic Oncology Group)といった多施設共同臨床研究グループにも当教室の代表として参画しています。

7. 進行卵巣癌に対する医師主導治験を実施しています
当院では、「血中循環腫瘍DNA陽性の腫瘍減量術後進行卵巣がん患者を対象としてベバシズマブ+ニラパリブ併用療法とニラパリブ単剤維持療法を比較する無作為化第Ⅱ相試験」を実施しております。
血中循環腫瘍DNA(circulating tumor DNA、以下ctDNA)は血液中に微量に存在する腫瘍由来のDNAです。リスク因子としてのctDNAの有用性を明らかにするとともに、再発高リスクと考えられる術前化学療法―腫瘍減量術後のctDNA陽性例に対して、現在の標準治療でありますPARP阻害薬ニラパリブ単剤での維持療法に比べてニラパリブ+ベバシズマブ併用の維持療法の効果があるかを検証します。
詳しくはPDFをご覧ください。
PDFはこちら
なお、本試験の詳細はjRCT(臨床研究実施計画・研究概要公開システム)で公開されています。計画番号はjRCT2031220732です。
https://jrct.niph.go.jp/latest-detail/jRCT2031220732